Contenido
Vacunas de Argentina 4
Virus Papiloma Humano (HPV)
Agente inmunizante:
- Están disponibles y licenciadas dos vacunas contra el VPH : una cuadrivalente, (Gardasil®) contra tipos de VPH 6 – 11 – 16 y 18 y la otra, bivalente, (Cervarix ®) contra los tipos de VPH 16 y 18.
- Ambas son preparadas por tecnología recombinante, utilizando proteínas estructurales L1 purificadas que son ensambladas en partículas símil virus (VLP).
- Ninguna contiene productos biológicos vivos ni ADN viral.
Indicaciones:
- Niñas de 11 años de edad nacidas a partir del 1° de enero del 2000.
- Indicada para la prevención del cáncer de cuello uterino por los tipos 16 y 18 de virus HPV, en mujeres entre los 9 y 13 años, previo al inicio sexual.
- Verrugas genitales.
- En el 2017 se incluyeron a los varones para la vacunación contra el VPH.
- Se aplica a todos los adolescentes (varones y mujeres) que cumplan 11 años en el 2017, es decir, los nacidos a partir del 1° de enero del 2006.
- Recordar que todas las niñas nacidas a partir del año 2000, deben completar sus esquemas de vacunación VPH.
Esquema:
- Vacuna Bivalente: el esquema recomendado es de 0, 1 y 6 meses. Si es necesario un esquema alternativo, la segunda dosis puede ser administrada entre 1 y 2 meses y medio posteriores a la 1a dosis.
- Vacuna Cuadrivalente: el esquema de vacunación consiste en 3 dosis, a aplicarse a los 0, 2 y 6 meses.
- Si es necesario un esquema de vacunación alternativo, la segunda dosis debe ser administrada al menos 1 mes después de la primera dosis y la tercera dosis debe ser administrada al menos 3 meses después de la segunda dosis.
- Las 3 dosis deben ser administradas dentro de un periodo de 1 año.
Dosis y Vía de Administración:
- Dosis: 0,5 ml.
- Vía: Intramuscular, en el deltoides.
- Luego de la aplicación la paciente deberá permanecer sentada y en observación por espacio de 15 minutos.
Conservación:
- Entre 2º y 8 °C.
- No congelar.
- Conservar en el envase original protegido de la luz.
Efectos adversos:
- Reacciones en el lugar de la inyección.
- Incluyendo dolor.
- Enrojecimiento.
- Tumefacción.
- Fiebre.
- Mialgias.
- Artralgias.
- Náuseas.
- Vómitos.
- Diarrea.
- Prurito.
- Erupción.
- Urticaria.
- Cefaleas.
Contraindicaciones:
- Hipersensibilidad conocida a cualquiera de los componentes de la vacuna.
- Embarazo.
- Lactancia.
Uso simultáneo con otras vacunas:
- Puede aplicarse simultáneamente; en sitios diferentes; con las vacunas del calendario nacional
Inmunocomprometidos: los pacientes con VIH y trasplantados hasta 26 años deben recibir la vacuna, con un esquema de 3 dosis.
Inmunoprofilaxis: No hay estudios que avalen la intercambiabilidad de las dos marcas.

Vacuna Sextuple (DTPa+Hib+HB+IPV)
Agente inmunizante:
Contiene: toxoide diftérico, toxoide tetánico, Antígenos de Bordetella pertussis: (toxoide pertussis, hemaglutinina filamentosa, pertactina), Antígeno de superficie del virus de la hepatitis B; Virus polio (inactivados) y Polisacárido de Haemophilus influenzae tipo b conjugado con toxoide tetánico, hidróxido de aluminio y fosfato de aluminio.
Presentación:
- Frasco ampolla conteniendo monodosis liofilizada (polvo blanco) de componente contra Hib, y jeringa prellenada conteniendo monodosis de la suspensión (blanca turbia) inyectable que contiene los componentes contra DTPa-HB- IPV.
Indicaciones:
- Indicaciones bajo programa en el sistema público: Recién nacidos prematuros < 1500 gr. nacidos a partir del 1-04-13, que sean menores de 6 meses al iniciar su esquema primario de vacunación.
- Con criterio individual puede utilizarse como esquema primario de vacunación.
Esquema:
- 3 dosis, a los 2, 4 y 6 meses de vida.
- Independientemente de la dosis de Hepatitis B aplicada al nacimiento.
- Intervalo mínimo entre dosis 8 semanas.
Dosis y Vía de Administración:
- Dosis: 0.5ml
- Vía y lugar de aplicación: IM profunda en cara anterolateral de muslo.
- Se sugiere cambiar los sitios de aplicación para las dosis subsiguientes.
Conservación:
- Entre 2 y 8 ° C.
- Proteger de la luz
Efectos adversos:
- Locales: induración, y más raramente: vesículas en el sitio de aplicación y edema del miembro.
- Generales: diarrea, vómitos, temperatura > a 39.5°C, somnolencia, inquietud.
Contraindicaciones:
- Reacción alérgica severa posterior a una dosis previa o a componentes de la vacuna.
- Encefalopatía de etiología desconocida en los 7 días siguientes a una vacunación anterior con componente pertussis.
- Se debe suspender la vacunación contra pertussis y la serie de vacunación se debe continuar con las vacunas antidiftérica, antitetánica, antihepatitis B, antipoliomielítica y anti-Hib.
Uso simultáneo con otras vacunas:
- Puede aplicarse simultáneamente con la vacuna antineumocócica conjugada.
Inmunocomprometidos: Puede ser aplicada a VIH.
Rotavirus
Agente inmunizante:
Hay dos presentaciones comerciales en monodosis:
- Vacuna de virus vivos atenuados humanos (monovalente), que contiene la cepa RIX4414, con especificidad G1P [8], derivada de la cepa de origen 89-12. Debe reconstituirse con un buffer de bicarbonato de calcio.
- Vacuna de cinco serotipos (pentavalente) a virus vivos atenuados, re asociada con virus bovino WC3 y proteínas de superficie de 5 serotipos humanos: G1, G2, G3, G4 y P [8]. No necesita ser reconstituida
Presentación:
- Vacuna monovalente: Rotarix® que contiene la cepa RIX4414, con especificidad G1P [8], derivada de la cepa de origen 89-12. La presentación líquida es en jeringa prellenada, para ser administrada por vía oral.
- Vacuna pentavalente: Rotateq® re asociada con virus bovino WC3 y proteínas de superficie de 5 serotipos humanos: G1, G2, G3, G4 y P [8]. No necesita ser reconstituida.
Indicaciones:
- Tener en cuenta que la edad mínima para recibir la primera dosis es de 6 semanas y la edad máxima para recibir la primera dosis es de 14 semanas y 6 días.
- No deben recibir ninguna dosis más allá del 8° mes.
- A partir del 1° de enero de 2015 se incorporó al Calendario Nacional de Vacunación la Vacuna contra el Rotavirus.
- Niños nacidos a partir del 1° de noviembre de 2014.
Esquema:
La recomendación actual para el uso de vacuna monovalente es:
- Esquema de dos dosis, que recibirán a los 2 y 4 meses de edad.
Las recomendaciones actuales para el uso de ambas vacunas son:
- N° de dosis 3 – 2.
- Edad para las dosis 2, 4 y 6 meses. 2 y 4 meses.
- Mínimo para la 1a dosis 6 semanas.
- Máximo para la 1a dosis 14 semanas 6 días.
- Mínimo intervalo entre dosis 4 semanas.
- Máxima edad para la 8 meses 0 días 8 meses 0 días última dosis.
Dosis y Vía de Administración:
- Dosis:
-monovalente: 1 ml.
-pentavalente: 2 ml. - Vía: Oral.
- Si el niño regurgita o vomita luego de la administración, no debe repetir la dosis.
Conservación:
- La monovalente se presenta en forma liofilizada, la pentavalente es líquida, ambas se conservan entre 2º y 8 ºC.
- La monovalente una vez reconstituida, entre 2 y 8 ºC, puede conservarse hasta 24 horas.
- No deben congelarse.
Efectos adversos:
- Irritabilidad.
- Falta de apetito.
- Diarrea.
- Vómitos.
- Fiebre.
- Fatiga.
Contraindicaciones:
- Reacción alérgica severa a alguno de los componentes de las vacunas.
- Enfermedad que compromete el estado general.
- Diarrea moderada a severa y/o vómitos.
- Historia previa de invaginación intestinal.
- Huéspedes inmunocomprometidos.
Uso simultáneo con otras vacunas:
- Ambas vacunas se pueden administrar con las otras vacunas de los esquemas regulares de vacunación.
- No son necesarias restricciones en la ingesta de alimentos o líquidos, incluyendo la lactancia materna.
-
Es importante no retrasar la aplicación de las dosis, ya que ésta vacuna tiene edades máximas y ya pasado ese tiempo no se pueden recibir.
Inmunocomprometidos:
- Contraindicada.
- Ambas vacunas pueden administrarse a convivientes con inmunosuprimidos.
Inmunoprofilaxis: No se ha evaluado la interferencia de la respuesta inmunitaria con la administración reciente de Ig. estándar o específica, o hemoderivados.

Varicela
Agente inmunizante: Vacuna viral atenuada. Se utiliza el virus varicela zoster cepa OKA atenuada, obtenida en células diploides humanas.
Indicaciones:
- Niños a partir de los 12 meses de edad, adolescentes y adultos sanos susceptibles.
- Contactos sanos susceptibles, convivientes de inmunocomprometidos y de prematuros menores de 1500 gr.
- Pacientes VIH asintomáticos o sintomáticos sin alteración de la inmunidad.
- en niños con CD4 > al 15% y en los adolescentes y adultos con CD4 > a 200/mm3.
- Pacientes con deterioro de la inmunidad humoral.
- Pacientes en programa de trasplantes de órganos sólidos por lo menos 1 mes antes del trasplante.
- Pacientes con leucemia, linfomas o tumores sólidos con remisión y 3 meses después de haber finalizado el tratamiento con quimioterapia.
- Pacientes con enfermedades crónicas que no reciban inmunosupresores o corticoides a dosis >2mg/kg/día por más de 15 días.
- Síndrome nefrótico.
- Inmunoprofilaxis: para prevenir o modificar la enfermedad puede utilizarse entre los 3 a 5 días del contacto.
Esquema:
- Niños entre 12 meses y 12 años:
Dos dosis de 0,5 ml para los que, por interrogatorio, resultaran susceptibles. La primera dosis, entre los doce a quince meses de vida, y la segunda, en la edad escolar, entre los 4 y 6 años (o cuando correspondiera), si bien esta última se puede administrar con un intervalo mínimo de tres meses con respecto a la primera dosis. - Personas desde los 13 años:
Dos dosis de 0,5 ml cada una, con un intervalo de cuatro a ocho semanas entre ambas. En este grupo se debe considerar primero la factibilidad de la realización de una prueba serológica para evaluar la inmunidad frente a VVZ si el antecedente de haber tenido la enfermedad fuera negativo o incierto
Dosis y Via de Administracion:
- Dosis: 0.5 ml
- Vía: Subcutánea
- Pacientes inmunocomprometidos. Dos dosis de 0,5 ml cada una, con un intervalo de cuatro a ocho semanas entre ambas; en pacientes con VIH, el intervalo entre dosis debe ser de tres meses.
Conservación:
- 2º y 8 ºC.
- No debe congelarse.
- Una vez reconstituida debe ser aplicada dentro de los 30 minutos.
Efectos adversos:
- Locales: eritema, tumefacción y dolor.
- Generales: rash variceliforme con pocas vesículas (2 a 15) en la primera semana.
- En inmunocomprometidos: fiebre y rash variceliforme en el 20-40%.
Contraindicaciones:
- Reacción alérgica severa a la vacuna o a algunos de sus componentes.
- Inmunodeficiencias severas.
- Pacientes VIH con CD4 <15%.
- Inmunodeficiencia celular
- Altas dosis de corticoides (2 mg/kg/día de prednisona o equivalente por más de 15 días).
- Embarazo o posibilidad de embarazo dentro del mes.
- Dentro de los 3 meses post radioterapia.
Uso simultáneo con otras vacunas:
- Se puede administrar con otras vacunas, en sitios diferentes.
- Si dos vacunas virales atenuadas parenterales, no se administran al mismo tiempo, se recomienda respetar un intervalo de 30 días entre dosis.
Inmunocomprometidos: Vacunar a los convivientes y a los VIH sintomáticos o asintomáticos con CD4 >15%.
Meningocócica Conjugada C
Agente inmunizante: Contiene oligosacáridos de meningococos del serogrupo C conjugado con Proteína CMR 197, de Corynebacterium difhtheriae (Menjugate®). O conjugada a la proteína de toxina tetánica (Neisvac-C®). Presenta Hidróxido de aluminio como adyuvante
Indicaciones:
- Brotes epidémicos: La autoridad sanitaria competente definirá la conducta que debe seguirse.
- Cuando se decida realizar la vacunación en una zona donde se comprueba un brote epidémico, la vacuna deberá seleccionarse de acuerdo con el serogrupo prevalente y el grupo etario más afectado.
- Poblaciones con mayor riesgo:
- Asplenia funcional o quirúrgica.
- Déficit de factores terminales del complemento.
- Huéspedes inmunocomprometidos.
- Viajeros a zonas endémicas/hiperendémicas.
- Personas que viven en comunidades semicerradas (estas dos últimas indicaciones no están contempladas para ser provistas por el Programa de Inmunizaciones).
Esquema:
- Niños < 12 meses: 2 dosis separadas por un intervalo mínimo de 1 mes. Con un refuerzo entre los 12 a 15 meses.
- Niños mayores de 12 meses, adolescentes y adultos: una única dosis de 0,5 ml.
Dosis y Vía de Administración:
- Dosis: 0,5 ml.
- Vía: Intramuscular.
Conservación:
- 2º y 8 ºC.
- No debe congelarse.
- Se podrá observar durante el almacenamiento un depósito blanco y un sobrenadante transparente.
- Antes de su administración, la vacuna deberá ser agitada para obtener una suspensión homogénea y además se deberá efectuar una inspección visual para observar la posible presencia de partículas extrañas y/o cualquier cambio en el aspecto físico.
- En tal caso, se deberá descartar la vacuna.
Contraindicaciones:
- Hipersensibilidad a algunos de los componentes del producto.
- Procesos febriles o enfermedades agudas que impliquen compromiso del estado general.
Inmunocomprometidos: Se puede utilizar aunque hay escasos datos sobre la inmunogenicidad y eficacia en estos pacientes.

Meningocócica Conjugada Tetravalente (ACW135Y)
Agente inmunizante: Contiene oligosacáridos de meningococos de serogrupos A; C; W-135 e Y, conjugada en forma monovalente con Proteína CMR 197, de Corynebacterium difhtheriae (MenACWY-CMR, Menveo®, Novartis).
Existe otra vacuna, también tetravalente que conjuga en forma monovalente con toxoide diftérico, los polisacáridos de meningococo A; C; W-135; Y (MenACWY-D, Menactra®, Sanofi Pasteur).
Provoca una respuesta de las células T que conducen a crear memoria inmunológica cuando entra en contacto con el germen.
Indicaciones:
- Pueden utilizarse con criterio individual.
- La vacuna Menveo® está licenciada a partir de los 2 meses de edad hasta los 65 años.
- La vacuna Menactra® está licenciada a partir de los 9 meses de edad hasta los 55 años.
- El Programa la provee para su uso en personas con factores de riesgo aumentado:
- Asplenia (anatómica o funcional).
- Déficit de factores terminales del Complemento (Déficit de Properdina, C3, factor D).
- VIH/Sida.
- Personal de laboratorio bacteriológico que procesa cultivos.
- Situación de brote epidémico con serogrupos que se encuentran en la vacuna.
- Indicación no provista por el Programa: viajeros a zonas hiperendémicas.
Esquema:
- Menveo®:
- Niños menores de 6 meses: 2, 4, 6 meses y refuerzo entre los 12-16 meses.
- Niños entre 6-23 meses: 2 dosis con intervalo de 8 semanas, la 2° a partir de los 12 meses.
- De 2 a 65 años: 1 dosis.
- Niños de 2 a 5 años con factores de riesgo 2 dosis separadas de 8 semanas.
- Menactra®:
- Niños de 9 a 23 meses: 2 dosis separadas de 3 meses.
- Personas sanas a partir de 2 años: 1 dosis
- Con factores de riesgo: 2 dosis separadas de 2 o 3 meses.
- De persistir con los factores de riesgo: dosis booster en < de 7 años a los 3 años; > 7 años una dosis cada 5 años.
Dosis y Vía de Administración:
- Dosis: 0.5 ml.
- Vía: Intramuscular.
Conservación:
- 2 y 8°C.
- Conservar en envase original protegido de la luz.
- Se presenta como suspensión blanca turbia.
- No congelar.
Efectos adversos:
- Reacciones en el lugar de inyección.
- Dolor.
- Enrojecimiento.
- Tumefacción.
- Induración.
- Fiebre.
- Mialgias.
- Náuseas.
- Malestar.
- Irritabilidad.
- Somnolencia.
- Cefaleas.
Contraindicaciones:
- Hipersensibilidad conocida a cualquiera de los componentes de la vacuna, incluyendo el toxoide diftérico.
- Enfermedad febril aguda grave.
- Embarazo y Lactancia: no hay datos suficientes para aconsejar su uso.
Inmunocomprometidos: Se puede utilizar aunque hay escasos datos sobre la inmunogenicidad y eficacia en estos pacientes.
Antirrábica de uso humano
Agente inmunizante:
- Las vacunas antirrábicas de uso humano emplean como agente inmunizante el virus rábico inactivado, que es un descendiente del virus fijo producido en el laboratorio por Luis Pasteur.
- Hay 2 tipos de vacunas:
a) Vacunas antirrábicas producidas en tejido nervioso de animales (Fuenzalida-Palacios).
b) Vacunas producidas en cultivo de líneas celulares: Vacuna antirrábica producida en células Vero (PVRV) y Vacuna antirrábica purificada producida en embrión de aves.
Actualmente: se utilizan en el Centro antirrábico del Hospital Durand las producidas en cultivo de líneas celulares.
Presentación:
- Vacunas antirrábicas producidas en tejido nervioso de ratón lactante de 1 día de vida (Fuenzalida-Palacios o CRL).
- Tiene validez un año a partir de su producción.
- Verorab ®: Vacuna antirrábica producida en células Vero, Cepa rabia PM/WI-38-1503. 2,5UI (0,5 ml)
- Rabipur ®: Vacuna antirrábica purificada cultivo primario de fibroblastos de pollo, Cepa Flury Lep 2.5 UI (1 ml.)
Indicaciones:
- Varía según el sitio de mordedura y la posibilidad de observación del animal.
- En la Ciudad de Buenos Aires, la persona mordida debe concurrir al Hospital Durand, Pabellón Romano, Centro de Rabia Humana, Av. Díaz Vélez 5044, de lunes a domingo de 8 a 20 horas.
- Con el número de causa que se le entregue concurrirá al Instituto de Zoonosis Luis Pasteur, Av. Díaz Vélez 4851, 4982 4504/8421/6666 con el animal para su evaluación.
Esquema:
- Si es Pre exposición: PRVR: 3 dosis (0-7-21 o 28 días)
- CRL: 4 dosis (0-2-4-14 o 0-7-28-90)
- En el caso Pos exposición: la cantidad de dosis, dependerá del lugar de la herida y del tipo de animal involucrado.
Dosis y Vía de Administración:
- Dosis:
Rabipur®:1 ml
Verorab®: 0.5ml - Vía de administración: PRVR: intramuscular. CRL: subcutánea
Conservación:
- 2 ° a 8° C, en la parte central de la heladera.
- No debe congelarse.
Efectos adversos:
- PRVR: fiebre, escalofríos, malestar general, astenia, cefalea, mareos, artralgias, mialgias, náuseas, vómitos.
- CRL: los accidentes neuro paralíticos (parálisis tipo Landry), dolor dorsolumbar.
Contraindicaciones: No tiene.
Uso simultáneo con otras vacunas:
- Las vacunas antirrábicas se pueden administrar simultáneamente con cualquiera de las otras vacunas actualmente en uso.
- Deben ser aplicadas en sitios diferentes.
Inmunoprofilaxis:
- Contacto con animal con IFI para Virus Rabia +
- Contacto con animal silvestre.
- Paciente inmunocomprometido.
- Accidentes de alto riesgo.
Inmunocomprometidos: Deben recibir esquema postexposición con IG específica.
Fiebre hemorrágica Argentina Candid #1
Agente inmunizante: Virus vivo atenuado Junín Cepa Candid #1.
Presentación: Frascos de liofilizado conteniendo 10 dosis de vacuna con una ampolla diluyente de 5,5 ml de agua estéril para inyectable.
Indicaciones: a partir de los 15 años de edad en el área endémica de la enfermedad de las provincias de Santa Fe, Córdoba, La Pampa y Buenos Aires.
Esquema:
- Dosis única a partir de los 15 años.
- La vacunación debe realizarse por lo menos un mes antes de una posible exposición.
Dosis y Vía de Administración:
- Dosis: única de 0,5 ml de producto reconstituido.
- Vía: Intramuscular en región deltoidea.
Conservación:
- Los frascos liofilizados se deben conservar desde la recepción en el vacunatorio entre -15 y -20 °C por el término de 1 mes.
- La ampolla de diluyente se conserva entre 2 y 8 °C.
- La vacuna liofilizada se debe reconstituir con su diluyente, asegurando su completa disolución.
- Una vez reconstituida, la vacuna debe utilizarse dentro de las 4 horas y conservarse en la heladera (entre 2 y 8 °C), no en el freezer.
Efectos adversos:
- Cefaleas.
- Decaimiento.
- Mialgia.
- Fiebre.
- Náuseas.
- Vómitos.
- Dolor retroocular.
- Mareos.
Contraindicaciones:
- Embarazo.
- Lactancia.
- Déficit inmunitario congénito o adquirido.
Uso simultáneo con otras vacunas: No se dispone de datos sobre las asociaciones vacunales posibles. Deberá aplicarse en esquema exclusivo para ella.
Inmunocomprometidos: Contraindicada.
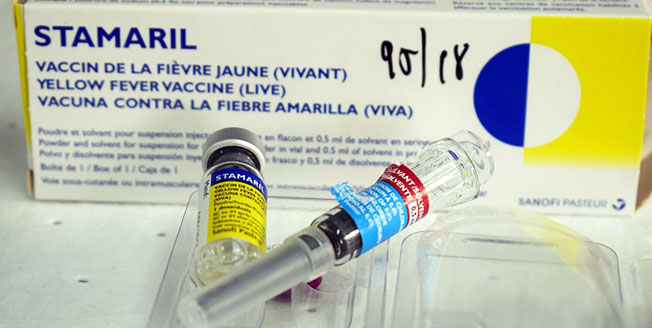
Fiebre amarilla (FA)
Agente inmunizante: Es una suspensión liofilizada de virus vivos atenuados de la cepa 17 D obtenida en huevos embrionados de pollo.
Presentación:
- La vacuna Stamaril®: se presenta en mono o multidosis.
- La monodosis se reconstituye con una jeringa que contiene solución fisiológica al 0.4%; la multidosis, con solución fisiológica al 0.9%, que se adjunta al envase.
- Una vez reconstituidas deben agitarse fuertemente hasta lograr su completa disolución, previo a su administración.
- La vacuna Bio-Manguinhos® se presenta como multidosis.
- El de 5 dosis se reconstituye con el diluyente (2,5 ml) suministrado por el productor.
- El de 50 dosis, con el frasco que contiene 25 ml. La reconstitución de esta presentación de 50 dosis se debe realizar en dos pasos: primero, la preconstitución de la vacuna liofilizada con un mililitro cúbico de diluyente, y segundo, el traspaso al frasco que contiene el resto de la solución.
- Hay que diluir lentamente con el diluyente, y se debe agitar el frasco reconstituido en forma suave y periódica.
- Una vez reconstituido es de color blanquecino y puede contener algunos filamentos.
- Es fundamental leer siempre el prospecto que acompaña a la vacuna.
- Después de la reconstitución, la vacuna debe mantenerse refrigerada a temperaturas entre 2 °C y 8 °C, puede utilizarse por un máximo de 6 horas después de su reconstitución.
Indicaciones:
Es una vacuna de reglamentación internacional que se indica a partir del año de edad a:
- Viajeros que ingresan o salen de zonas endémicas o epidémicas.
- Residentes de zonas endémicas o epidémicas infestadas por el mosquito Aedes aegypti.
- Población de departamentos limítrofes con áreas de riesgo (Brasil, Bolivia y Paraguay).
- Recordar que la vacunación debe realizarse al menos 10 días previos al viaje.
- Es conveniente aplicarla por lo menos 10 días antes de exponerse al riesgo de infección.
Esquema:
- Se aplicará una dosis entre 1 y 60 años.
- No son necesarias las re vacunaciones.
- El reglamento sanitario internacional establece que en los casos en que la vacuna es obligatoria se re vacune cada 10 años.
- En situaciones especiales se puede considerar disminuir la edad de aplicación.
Dosis y Vía de Administración:
- Dosis: 0,5 ml.
- Vía: Subcutánea o intramuscular
Re vacunación:
El reglamento sanitario internacional establece que en los casos en que la vacuna es obligatoria se re vacune cada 10 años.
Conservación:
- Debe conservarse entre 2 ºC y 8ºC, protegida de la luz.
- No debe congelarse.
- Luego de reconstituida permanece viable por seis horas.
- Agitar antes de aplicar.
- El diluyente se almacena a temperatura ambiente, pero para reconstituir debe estar a la misma temperatura de la vacuna.
- Las ampollas del diluyente se pueden colocar en la heladera un día antes de usarlo.
- Sólo se utilizará el diluyente suministrado por el fabricante de la vacuna.
- La utilización de otro diluyente puede dañar la vacuna, inactivando el virus vacunal.
Efectos adversos:
- Cefalea.
- Fiebre.
- Malestar general.
- Reacción local en el sitio de la inyección.
Contraindicaciones:
- Menores de 6 meses.
- Hipersensibilidad a los huevos, proteínas de pollo o cualquier componente de la vacuna.
- Reacciones graves de hipersensibilidad (anafilaxia) después de una dosis anterior de vacuna de fiebre amarilla.
- Huéspedes con inmunodeficiencia (congénita, idiomática, por consecuencia de un tratamiento inmunosupresor, infección sintomática o asintomático por VIH).
- Enfermedad febril aguda.
- Antecedentes de patología del timo.
Precauciones:
- En lo posible, no vacunar durante el embarazo. De ser necesario, se puede aplicar después del 6º mes de embarazo.
- Los niños de edad comprendida entre 6 y 12 meses sólo deben ser vacunados en circunstancias especiales (por ejemplo grandes epidemias y en base a las recomendaciones vigentes).
- Personas de edad igual o superior a los 60 años.
- Mujeres que están en período de lactancia entre el nacimiento y los 8 meses inclusive podrían transmitir a sus hijos el virus vacunal a través de la leche.
- Alteraciones del sistema inmune incluyendo la infección por VIH según recuento de linfocitos T CD4+.
Uso simultáneo con otras vacunas:
- La vacuna contra la fiebre amarilla se puede administrar simultáneamente con cualquier vacuna, incluso con otras vacunas inyectables de virus vivos atenuados (sarampión, rubéola, paperas, varicela) siempre y cuando sean aplicadas en sitios diferentes.
- Si no se administra simultáneamente con las vacunas inyectables de virus vivos, se deberá aplicar respetando un intervalo mínimo de 4 semanas.
- La única excepción es la vacuna contra el cólera inactivada, que no se debe administrar simultáneamente con la vacuna antiamarílica.
- Deben ser aplicadas con un intervalo de por lo menos 3 semanas para que generen una buena respuesta inmunitaria.
- Se puede administrar la vacuna antiamarílica a personas que reciben profilaxis antimalaria, no afectándose la respuesta inmunitaria.
- Las gammaglobulinas no interfieren la respuesta inmunitaria de la vacuna.
Inmunocomprometidos: No debe aplicarse.
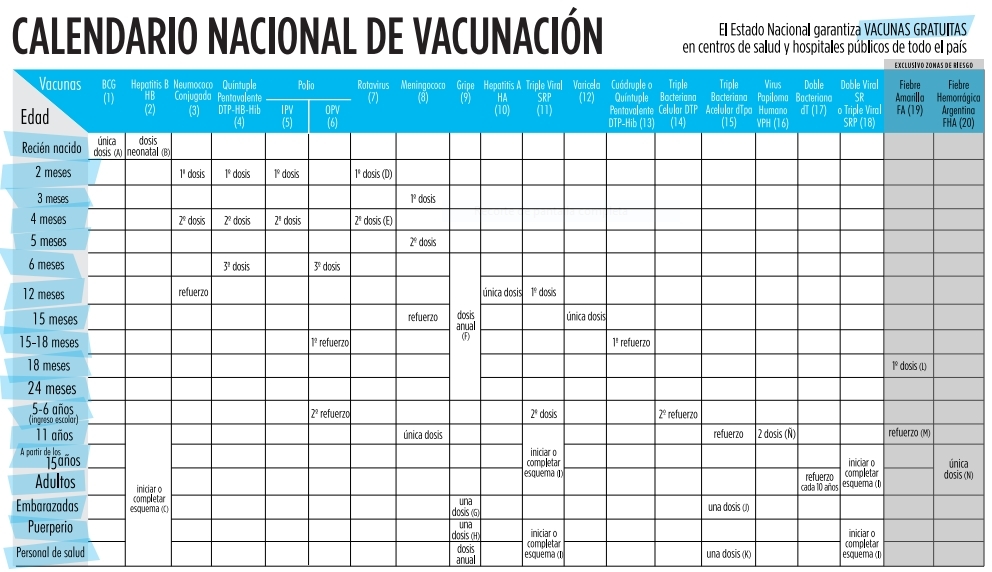
Calendario Nacional de Vacunación
Recomiendo el siguiente artículo: Diferencias de vacunas entre Argentina – España – Estados Unidos
Link de interés:
Para consultar esquemas de vacunación de otros países:
www.who.int/vaccines/globalsummary/immunization/ScheduleSelect.cfm
Para consultas de vacunas en general:
www.salud.buenosaires.gob.ar (Ministerio de Salud de la Ciudad de Buenos Aires)
www.msal.gov.ar (Ministerio de Salud de la Nación)
Para consultas de Medicina del Viajero:
Hospital Muñiz. Uspallata 2272, Sala 9, Pabellón 30, 4304-2180/0335, int. 231
www.cdc.gov/travel
www.who.int/ith/
Para aplicación de vacuna contra la fiebre amarilla:
Dirección de Sanidad de Fronteras, Av. Ingeniero Huergo 690, 4343-1190
Información del autor
- https://www.buenosaires.gob.ar
- Lorena Plazas. Lic. en enfermería. Trabajo propio.
- https://www.buenosaires.gob.ar/hospitalfernandez/vacunacion. Imagen portada
Última actualización: [04/04/2023]

Trastorno de Oposición Desafiante en niños ¿Cómo identificarlo?

Diferencia entre Nutrición Comunitaria y Educación Alimentaria
Escala Canadiense: Utilidad, Interpretación y Aplicaciones Clínicas

Raciones para Dieta Hipocalórica

Que es la alimentación hedónica

Tos nerviosa o seca: ¿Qué la diferencia de otros tipos de tos?

Enfermería empírica

Maltrato en pacientes vulnerables
La enfermería como defensora de los derechos del paciente