Teorías del Desarrollo
Este artículo explorará las Teorías del Desarrollo, en consonancia con el contenido de la Unidad 2, “Desarrollo de la Identidad”, de la materia Proceso de Desarrollo de la Persona. Este análisis se enmarca dentro del programa de la Licenciatura en Enfermería de la Escuela Nacional de Enfermería y Obstetricia (ENEO) de la Universidad Nacional Autónoma de México (UNAM).
El estudio del desarrollo humano es un pilar fundamental de la psicología. Busca comprender cómo cambian las personas a lo largo de su vida, desde la infancia hasta la vejez. Las “teorías del desarrollo” proporcionan marcos conceptuales para interpretar estos cambios, ofreciendo perspectivas sobre los factores que influyen en el crecimiento, la maduración y la adaptación. Este artículo explora algunas de las teorías del desarrollo más influyentes, destacando sus contribuciones y diferencias clave.
El mosaico teórico del desarrollo
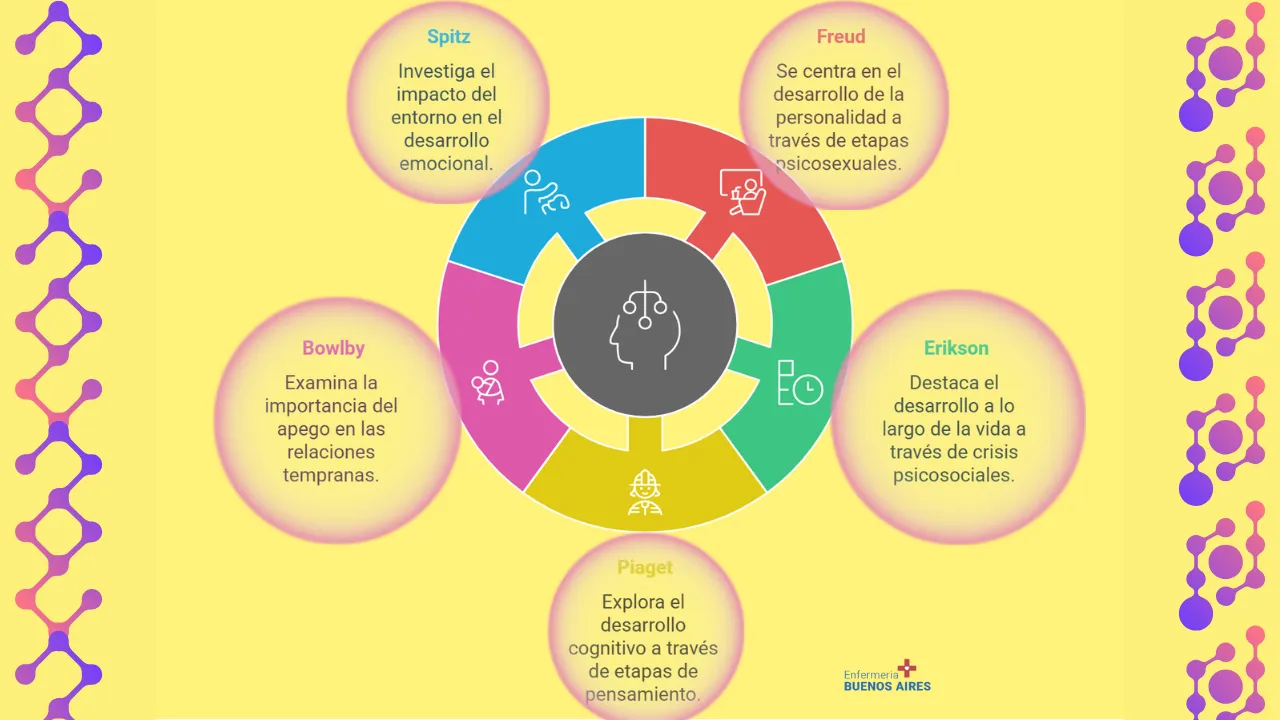
Existen numerosas teorías que intentan explicar el desarrollo humano, cada una con un enfoque particular en diferentes aspectos de la experiencia. A continuación, examinaremos cinco teorías que han tenido un impacto significativo en la comprensión del desarrollo:
- Teoría del Desarrollo Psicosexual de Sigmund Freud
- Teoría Psicosocial de Erik Erikson
- Teoría del Desarrollo Cognoscitivo de Jean Piaget
- Teoría del Apego de John Bowlby
- Teoría de los Organizadores de la Personalidad de René Spitz
1.Teoría del Desarrollo Psicosexual de Sigmund Freud
Sigmund Freud, el padre del psicoanálisis, propuso una teoría del desarrollo psicosexual que se centra en cómo las experiencias de la infancia temprana moldean la personalidad adulta. Freud creía que la libido, o energía sexual, se enfoca en diferentes zonas erógenas del cuerpo durante distintas etapas del desarrollo. Estas etapas son:
-
Etapa oral (0-18 meses): el placer se centra en la boca a través de actividades como succionar, morder y comer. La fijación en esta etapa puede llevar a la dependencia o la agresividad en la edad adulta.
-
Etapa anal (18 meses-3 años): el control de los esfínteres se convierte en una fuente de placer y conflicto. La fijación puede resultar en la obstinación o la compulsividad.
-
Etapa fálica (3-6 años): los niños se vuelven conscientes de sus genitales y experimentan el complejo de edipo (amor por el progenitor del sexo opuesto y rivalidad con el del mismo sexo) o el complejo de electra en las niñas. La resolución exitosa de esta etapa lleva a la identificación con el progenitor del mismo sexo y al desarrollo del superego.
-
Periodo de latencia (6 años-pubertad): la energía sexual se reprime y los niños se enfocan en el desarrollo de habilidades sociales e intelectuales.
-
Etapa genital (pubertad en adelante): la libido se dirige hacia las relaciones sexuales maduras.
La teoría de Freud, aunque controvertida, destaca la importancia de las experiencias tempranas y los impulsos inconscientes en la formación de la personalidad.
2.Teoría Psicosocial de Erik Erikson
Erik Erikson, un discípulo de Freud, expandió la teoría psicoanalítica para incluir el desarrollo psicosocial a lo largo de toda la vida. Erikson propuso que en cada etapa del desarrollo, las personas enfrentan una crisis psicosocial que deben resolver para desarrollar un sentido saludable de sí mismos. Estas crisis son:
-
Confianza vs. desconfianza (0-18 meses): los bebés aprenden a confiar en sus cuidadores si sus necesidades son satisfechas de manera consistente.
-
Autonomía vs. vergüenza y duda (18 meses-3 años): los niños pequeños exploran su independencia y aprenden a controlar sus cuerpos.
-
Iniciativa vs. culpa (3-6 años): los niños en edad preescolar toman la iniciativa y aprenden a planificar y llevar a cabo tareas.
-
Laboriosidad vs. inferioridad (6-12 años): los niños en edad escolar desarrollan habilidades y aprenden a cooperar con otros.
-
Identidad vs. confusión de roles (adolescencia): los adolescentes exploran diferentes roles e identidades para formar un sentido coherente de sí mismos.
-
Intimidad vs. aislamiento (adultez joven): los adultos jóvenes buscan relaciones íntimas y comprometidas.
-
Generatividad vs. estancamiento (adultez media): los adultos de mediana edad se preocupan por contribuir a la sociedad y criar a la siguiente generación.
-
Integridad vs. desesperación (vejez): los ancianos reflexionan sobre sus vidas y buscan un sentido de integridad y satisfacción
La teoría de Erikson enfatiza la importancia de las interacciones sociales y culturales en el desarrollo de la personalidad a lo largo de la vida.
3.Teoría del Desarrollo Cognoscitivo de Jean Piaget
Jean Piaget, un psicólogo suizo, se centró en cómo los niños construyen su conocimiento del mundo a través de la exploración y la experiencia. Piaget propuso que el desarrollo cognoscitivo ocurre en cuatro etapas:
-
Etapa sensoriomotora (0-2 años): los bebés aprenden sobre el mundo a través de sus sentidos y acciones. Desarrollan la permanencia del objeto (la comprensión de que los objetos siguen existiendo aunque no estén a la vista).
-
Etapa preoperacional (2-7 años): los niños desarrollan el pensamiento simbólico y el lenguaje, pero su pensamiento es egocéntrico y carece de lógica.
-
Etapa de operaciones concretas (7-12 años): los niños desarrollan el pensamiento lógico sobre objetos y eventos concretos. Pueden comprender la conservación (la comprensión de que la cantidad de un objeto no cambia aunque su apariencia cambie).
-
Etapa de operaciones formales (12 años en adelante): los adolescentes desarrollan el pensamiento abstracto y la capacidad de razonar hipotéticamente.
La teoría de piaget destaca la importancia de la interacción activa del niño con su entorno en la construcción del conocimiento.
4.Teoría del Apego de John Bowlby
John Bowlby, un psiquiatra y psicoanalista, desarrolló la teoría del apego para explicar cómo los vínculos emocionales tempranos entre los bebés y sus cuidadores influyen en el desarrollo social y emocional.
Bowlby creía que los bebés tienen una necesidad innata de formar un apego seguro con un cuidador principal para sobrevivir. Los patrones de apego que se desarrollan en la infancia temprana tienden a persistir a lo largo de la vida y a influir en las relaciones adultas. Mary Main y sus colegas desarrollaron el “Adult Attachment Interview” para evaluar los patrones de apego en adultos.
Los cuatro patrones de apego principales son:
-
Apego seguro: los bebés se sienten seguros y protegidos por sus cuidadores y confían en que estarán disponibles cuando los necesiten. Los adultos con apego seguro tienden a tener relaciones saludables y satisfactorias.
-
Apego ansioso-ambivalente: los bebés se muestran ansiosos y ambivalentes hacia sus cuidadores, buscando cercanía pero resistiéndose al contacto. Los adultos con apego ansioso-ambivalente tienden a ser inseguros y demandantes en sus relaciones.
-
Apego evitativo: los bebés evitan el contacto con sus cuidadores y no muestran angustia cuando se separan de ellos. Los adultos con apego evitativo tienden a ser distantes y a evitar la intimidad en sus relaciones.
-
Apego desorganizado: los bebés muestran comportamientos confusos y contradictorios hacia sus cuidadores, a menudo como resultado de experiencias de trauma o abuso. Los adultos con apego desorganizado tienden a tener dificultades para regular sus emociones y mantener relaciones estables.
La teoría del apego destaca la importancia de las relaciones tempranas en el desarrollo emocional y social.
5.Teoría de los Organizadores de la Personalidad de René Spitz
René Spitz, un psicoanalista, propuso la teoría de los organizadores de la personalidad, que se centra en cómo las experiencias tempranas y las relaciones interpersonales moldean el desarrollo de la personalidad. Spitz creía que el desarrollo ocurre en etapas, cada una marcada por la aparición de un “Organizador” psicológico que integra las experiencias anteriores y prepara al niño para la siguiente etapa.
Los tres organizadores principales son:
-
La sonrisa social (alrededor de los 3 meses): la sonrisa social indica que el bebé ha desarrollado la capacidad de reconocer y responder a los rostros humanos, lo que facilita la interacción social y el apego.
-
La angustia ante el extraño (alrededor de los 8 meses): la angustia ante el extraño indica que el bebé ha desarrollado la capacidad de distinguir entre personas familiares y desconocidas, lo que refleja el establecimiento de un vínculo de apego seguro con el cuidador principal.
-
El “no” semántico (alrededor de los 15 meses): el “no” semántico indica que el niño ha desarrollado la capacidad de comprender y utilizar el lenguaje para expresar su voluntad y oponerse a las demandas de los demás, lo que marca el inicio de la autonomía y la individuación.
La teoría de Spitz destaca la importancia de las relaciones interpersonales tempranas en el desarrollo de la personalidad y la capacidad de adaptación social.
Conclusión
Las teorías del desarrollo ofrecen perspectivas valiosas sobre cómo cambian las personas a lo largo de la vida. cada teoría tiene sus fortalezas y limitaciones, y ninguna teoría por sí sola puede explicar completamente la complejidad del desarrollo humano.
Sin embargo, al combinar las ideas de diferentes teorías, podemos obtener una comprensión más completa y matizada de cómo las experiencias, las relaciones y los procesos biológicos interactúan para moldear quiénes somos. El estudio de las teorías del desarrollo es esencial para los profesionales de la salud mental, los educadores y cualquier persona interesada en comprender el potencial humano y promover el bienestar a lo largo de la vida.
Información del Autor
- Lorena Plazas. Lic. en enfermeria. Trabajo Propio
Fuentes bibliográficas
- Carver C, Sheier F. M. Teorías de la personalidad. 7a ed. EUA: Pearson;2014.
Última actualización: [05/03/2025]